AstraZeneca и Daiichi Sankyo: Направленное на дальнейшее расширение применения препарата Datroway для лечения рака молочной железы
AstraZeneca (AZN) и ее партнер из Японии, компания Daiichi Sankyo, объявили о том, что Управление по контролю за продуктами и лекарствами США (FDA) приняло и предоставило приоритетный пересмотр их дополнительной заявки на биологическую лицензию (sBLA) с целью одобрения противоопухолевого антитела-конъюгата (ADC), Datroway (датоэптамаб дерукстекан), для расширенного использования в лечении рака молочной железы.
Согласно полученному сообщению, FDA также направило AstraZeneca полное письмо с ответом (CRL) по заявке на одобрение подкожной (SC) формулы препарата Saphnelo (анифролумаб) для лечения взрослых пациентов с системной красной волчанкой (СКВ). На данный момент Saphnelo доступен на рынке в виде внутривенной инфузии в различных странах, включая США, страны Европейского Союза и Японию, для лечения пациентов с умеренной и тяжелой степенью заболевания.
Datroway: Шаг к новому лечению для пациентов с недостаточностью терапии PD-1/PD-L1
Заявка на одобрение Datroway касается лечения взрослых пациентов с неоперабельным или метастатическим тройным негативным раком молочной железы (TNBC), не подходящих для терапии ингибиторами PD-1/PD-L1. AstraZeneca уже использует Datroway на глобальном уровне для лечения взрослых пациентов с неоперабельным или метастатическим HR-положительным, HER2-отрицательным раком молочной железы после предыдущей эндокринной терапии и химиотерапии.
FDA предоставила приоритетный пересмотр данной заявки, ожидая завершения процесса во втором квартале 2026 года. Эта инициатива поддержки со стороны регулирующего органа подтверждается результатами исследования TROPION-Breast02 III фазы, где были продемонстрированы статистически значимые и клинически значимые улучшения в общей выживаемости и снижении риска прогрессирования заболевания или смерти по сравнению с традиционной химиотерапией при использовании в качестве первой линии лечения. Datroway также продемонстрировала более высокий объективный коэффициент ответа и продолжительность действия по сравнению с химиотерапией.
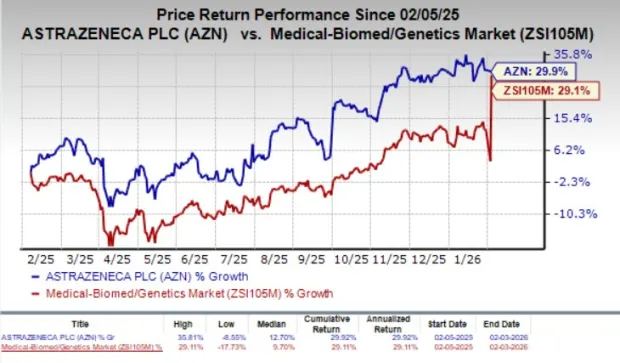
За последний год акции AstraZeneca повысились на 29,9%, что превосходит на 0,8% рост в среднем по отрасли, составивший 29,1%.
Помимо рака молочной железы, Datroway также одобрен в США по ускоренной программе для взрослых с локально распространенным или метастатическим немелкоклеточным раком легкого с мутациями EGFR, которые прогрессировали после терапии, направленной на EGFR, и платиновой химиотерапии. Препарат активно исследуется в рамках нескольких поздних клинических испытаний по различным онкологическим заболеваниям, включая рак легкого, молочной железы и уробластомы.
Совместная разработка Datroway осуществляется AstraZeneca и Daiichi Sankyo с 2020 года, где Daiichi Sankyo отвечает за производство и поставки.
Полное письмо с ответом FDA к AstraZeneca по Saphnelo
FDA направило полное письмо с ответом по биологической лицензии, поданной AstraZeneca, касающейся подкожной формы Saphnelo. Заявка основывалась на промежуточных данных III фазы TULIP-SC, которые показали безопасность препарата, соответствующую внутривенной инфузии Saphnelo.
Данные события подчеркивают динамику развития компании AstraZeneca на фармацевтическом рынке и ее стремление расширить арсенал лекарств для онкологических заболеваний. Это в свою очередь может сыграть важную роль в улучшении результатов лечения, особенно среди тех пациенток, которые сталкиваются с ограниченными вариантом выбора в текущих клинических практиках.